مسببات، التصنيف، الصورة السريرية، التشخيص والعلاج من سرطان الدم النذوي الحاد.
المحتوى
 سرطان الدم الحاد — مجموعة غير متجانسة من كلونال
سرطان الدم الحاد — مجموعة غير متجانسة من كلونالأمراض الورم من النسيج الهيماتيون يتميز بالرقابة
انتشار وتعطيل التمايز والتراكم في نخاع العظم و
الدم الطرفي من الخلايا المكونة للدم وغير الناضجة.
سرطان الدم الحاد هو 2-3٪ أورام خبيثة
رجل. حدوث سرطان الدم الحاد هو متوسط 3-5 حالات
100،000 السكان. في 75٪ من الحالات، يتم تشخيص المرض في البالغين، 25٪
حالات — عند الأطفال. متوسط نسبة سرطان الدم النذوي و Lymphoid
هو 6: 1. في المرضى البالغين الذين تزيد أعمارهم عن 40 عاما من 80٪ من الحالات
المقدمة من أشكال النخاع، في الأطفال — 80-90٪ — اللمفاوية. الوسيط
مرضى العمر مع سرطان الدم غير الحاد غير الحاد — 60-65 سنة، حاد
سرطان الدم الليمفاوي — 10 سنوات.
هناك احتمال وراثي للنامية الحادة
mylioid Leukoza. هناك عدد كبير من قضايا الأسرة تقارير
الأمراض، احتمالية IML لأقرب أقارب المريض
ثلاثة أعلاه. عدد من الدول الفطرية يمكن
زيادة احتمالية OML. في معظم الأحيان هو متلازمة داون، حيث يتم رفع احتمال IML في
10 — 18 مرة.
بعض المواد المسرطنة
(تسبب وكلاء الأورام) يمكن اعتبارها عوامل مسبقة
OML، مثل البنزين، التبغ التدخين والإشعاع المؤين. الأهم
عامل خطر أكبر من 65 سنة.
تأثير الفرد
السمات الوراثية للجسم، وكذلك التأثير على جسم خارجي
تظهر العوامل نفسها في تطوير سرطان الدم النخاعي الحاد الثانوي,
مكونات 5-20٪ من جميع حالات IML. على وجه الخصوص، قد يطور IML
الناس يخضعون سابقا للعلاج مع مواقع العلاج الكيميائي المختلفة
تشكيلات خبيثة أخرى.
وجود المرحلة السابقة في
شكل متلازمة MyLodSplastic (MDS) الأكثر شيوعا في كبار السن
المرضى أيضا، هو عامل خطر مهم OML. مضادوموريان
الآثار الكيميائية، وخاصة الأدوية الأليفة، أنثراسيق
و epipodophillexins، يزيد من احتمال تطور الثانوي
OML / Secondary MDS. أعلى احتمال المرض يقع لمدة 3-5 سنوات
بعد العلاج الكيميائي. تطبيق مجتمعة من العلاج الكيميائي / الإشعاع هو أيضا بشكل كبير
يزيد من خطر الإطارات الثانوية IML / MDS الثانوية. تجدر الإشارة إلى أن الثانوي
سرطان الدم / MDS تنشأ ليس في جميع المرضى الذين يتلقون المستانع
علاج او معاملة.
سرطان الدم الحاد هو
وبالتالي الضرر — الطفرات — في المواد الوراثية من استنساخ
خلايا المتطرفة. نتيجة لذلك، يحدث المستوى الجزيئي
الأحداث التي تؤدي إلى انتهاك للسيطرة على دورة الخلية، والتغيير
عمليات النسخ والمنتجات لعدد من منظمات البروتينات الرئيسية. خبيث
meloblasts تبرز الخلايا مع OML,
غير قادر على النضوج والتمايز نتيجة ضعف
التحكم الوراثي والتراكم
في نخاع العظام. خلايا Lakeclone
تتداخل مع أنشطة الخلايا العادية، دفعها من نخاع العظام.
جميع حاليا شارب
يتم اتخاذ سرطان الدم للتقسيم على سرطان الدم اللمفاوي الليمفاوي الحاد.
تم تقديم تصنيف سرطان الدم النذوي الحاد الذي تم عرضه أدناه.
تصنيف منظمة الصحة العالمية سرطان الدم النذوي
| اسم السلاح | وصف |
| OML S التغييرات الوراثية المميزة |
في المرضى الذين يعانون من مثل هذه السلطات الفرعية من IML عادة ما تكون مستويات عالية من مغفرة وتوقعات أفضل نسبيا مع OML من الآخرين السلالات. |
| OML مع خلل التنسج عدة روستكوف | هذه الفروض يشمل المرضى الذين يعانون من متلازمة myelodsplastic السابقة (MDS) أو مرض مايلوبروليفي (MPB), التي تذهب إلى IML. هذه الشكليات من IML هي أكثر شيوعا في كبار السن و يختلف التوقعات غير المواتية. |
| OML I MDS المرتبطة العلاج السابق | هذه الفروض يتضمن OML المرضى الذين يتلقون الكيمياء و / أو علاج الإشعاع بعد الذي جاء IML أو MDS. مع هذه اللوكيميا، قد تكون هناك سمة التغييرات في الكروموسومات، توقعاتها غالبا ما تكون أسوأ. |
| OML، N يخضع لعلامات الشركات الصغيرة المدرجة | يشمل OML الفرح غير المدرجة في تلك المذكورة أعلاه. |
فرانكو أمريكا البريطانية
تصنيف
تصنيف فرانكو الأمريكي البريطاني (FAB)
يشارك النظام IML إلى 8 فرص فرعية، من M0 بواسطة M7، بناء على الأنواع
خلايا — سلفات البيض، وعلى درجة نضج التغيير
خلايا. يتم تحديد الخلايا الخبيثة على أساس
علامات خارجية مع المجهر الخفيف و / أو التدليك الخلوي، والكشف عن
الانحرافات الأساسية للتغيرات في الكروموسومات. شركات مختلفة من IML
توقعات مختلفة والاستجابة للعلاج. على الرغم من مزايا تصنيف منظمة الصحة العالمية,
لا يزال نظام FOB يستخدم على نطاق واسع. بواسطة fab هناك ثمانية فرعية
األمن.
| السلالات | اسم | التغييرات citogenetic |
| M0 | متباينة الحد الأدنى سرطان الدم الخيري الحاد | |
| M1 | حار سرطان الدم myeloblastic دون النضج | |
| M2 | حار سرطان الدم Myeloblastic مع نضج من الحبيبات | T (8؛ 21) (Q22؛ Q22), ر (6؛ 9) |
| M3 | بروميلوكيرتار, أو بروميلوكيرتار الحاد سرطان الدم (أرضية المرجع) | ر (15؛ 17) |
| M4 | حار سرطان الدم المايلوموسي | Inv (16) (P13Q22), ديل (16Q) |
| M4eo | mylonocital جنبا إلى جنب مع النخاع العظمي الحيor | Inv (16), T (16؛ 16) |
| M5 | حظيرة حادة سرطان الدم (M5A) أو الحادة سرطان الدم الأحادي (M5B) (M5B) | ديل (11Q), T (9؛ 11)، ر (11؛ 19) |
| M6 | حار الحار سرطان الدم، بما في ذلك سرطان الدم الإرياني (M6A) ونظافة نادرة جدا سرطان الدم الإريثيتيد (M6B) | |
| M7 | حار سرطان الدم Megakaryoblastic | ر (1؛ 22) |
| M8 | البازفة الحادة سرطان الدم |
الصورة السريرية
يتم تحديد الصورة السريرية لسرطان الدم الحاد بسبب شدة
المتلازمات الأساسية:
- ويكيميم — انخفاض مستويات الهيموغلوبين و
عدد كريات الدم الحمراء، التي تتجلى
ضعف، انخفاض في القدرة العاملة، النعاس، المظاهر
قصور القلب، نبضات القلب,
ضعف، ضيق في التنفس، شحوب الجلد والأغشية المخاطية، العظام
انخفاض ضغط الدم، الذبحة الصدرية الثانوية واحتشاء عضلة القلب، ذكي
Chromota، عيادة الفشل التنفسي في المرضى الذين يعانون من مزمن
الأمراض الرئوية Broncho (COPD). - granulocytopenic — مضاعفات معدية,
بسبب انخفاض في عدد الحبيبات في الدم، الذي يتجلى ارتفاع درجة الحرارة والتسمم، وكذلك
العيادة المحلية (المناطق النخرية، التهاب الفم التقرحي، التهاب العظم والنقي
فكي بعد استخراج الأسنان) أو المعمم (تعفن الدم، التهاب الشد المعدي),
في كثير من الأحيان البكتيريا، العدوى. - النزفية
— نزيف في الجلد والمخاط، والنصف والنزف,
نزيف الجهاز الهضمي والكولي، نزيف الرحم، مرتفعة
BloodCaction أثناء التدخلات التشغيلية. - انتشار
— Lymphadenopathy، Splenomegaly، الكبد hepatomegaly، التهاب اللثة,
آلام في العظام، واضطرابات وظيفة أعصاب الدماغ الجمجمة، والصداع، والانتهاكات
الرؤية والعصبية العامة والتركيز
أعراض، صداع، priapism. - التاسين
— ضعف، انخفاض في الشهية، وفقدان الوزن، التعرق.
تشخيص سرطان الدم الحاد
 أولا
أولا
خطوة في التشخيص هو
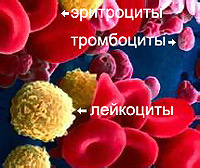
التحليل السريري للدم من خلال أخذ عينة الدم من الأوردة. في الدم عينة
يتم تحديد عدد خلايا الدم (كريات الدم الحمراء، والكريات البيض وسلعيتها، و
الصفائح الدموية أيضا). عندما الاكتشاف في التحليل السريري للدم أكثر من 20٪
يمكن تشخيص خلايا الانفجار بسرطان الدم الحاد.- في
عدم وجود دم كافي لتشخيص عدد الانفجارات، وكذلك
الغرض من التحقق الدقيق للتشخيص باستخدام طرق إضافية
تظهر الدراسات إجراء خزعة الطموح من نخاع العظم.
تشمل دراسة نخاع العظام دراسة نضح نخاع العظام
(تحليل امتحان الخلط الخلوي الخاص بي)، في حالات نادرة، يتم تنفيذه
نخاع العظم للحصول على دراسة نسيجية للنخاع العظمي. - في
جودة طرق البحث الإضافية لتحديد البديل الحاد
يتم تنفيذ سرطان الدم والعلامات النذير:
- cytoochemalical
البحث (المايلوبيرسيدي، إيسراز، جليكوجين) - cytogenetic
دراسة — الكشف عن الشذوذ للكروموسومات، مثل غياب أو
كروموسومات إضافية في خلايا نخاع العظام عن طريق التحليل القياسي
Metafaz أو طريقة الأسماك
(فلوري
في. التهجين
الموقع — الطريقة القائمة على القدرة
الحمض النووي للكروموسوم (الهدف) للاتصال بموجب شروط معينة مع الصغيرة
تسلسل الحمض النووي (تحقيقات)، تكميلية هذا الحمض النووي للكروموسوم. في
الانضمام إلى مسبار مادة الفلورسنت تنتج تحليل الحمض النووي من قبل
موقع الخلايا في خلايا التشابك). نتائج التدليك الخلوي
ترتدي الدراسات ذات الأهمية التشخيصية.
| exodus | انحراف | بقاء 5 سنوات | تردد recurious |
| ملائم | ر (8؛ 21), T (15؛ 17)، Inv (16) | 70٪ | 33٪ |
| مرض | لا كشفت، +8، +21، +22، ديل (7Q)، ديل (9Q)، انتهاكات 11Q23، كل الآخرين التغييرات الهيكلية أو العددية | 48٪ | خمسون٪ |
- البيولوجية الجزيئية
البحث (يتم إجراء البحوث الوراثية لتحديد المميزة
الطفرات التي يمكن أن تؤثر على نتيجة المرض — على سبيل المثال، Kinase FLT3-Tyrosine Kinase، جين CD117، متقاعد لتوليف المستقبلات
عامل نمو الخلايا الجذعية C- كيت، جينات السريعة,
BAALC، ERG، NPM1. - يذاكر
على خلايا الورم من المستضدات التفاضلية (CD) عن طريق التدفق الخلوي (المناعة المنحي).
في المستقبل في المرضى الذين يعانون من حاد
سرطان الدم إعادة دراسات نخاع العظام من أجل
تحديد تأثير العلاج، واكتمال المغفرة المحققة ومرحلة العملية
(مغفرة، الاستقرار، التقدم).
المراحل السريرية ومراحل المرض
- النشاط الابتدائي
المسرح — الفاصل الزمني بين المظاهر السريرية الأولى
الأمراض والتشخيص وأول مغفرة كاملة - ممتلئ
مغفرة الدم السريري — عدد خلايا الانفجار في المايلوجرام
ينخفض أقل من 5٪، لا توجد بؤر لكمي فيزا إضافي
الآفات، بينما في الدم المحيطي لا ينبغي أن يكون خلايا الانفجار,
عدد الصفائح الدموية 100×109 / L الوعاء البيضاء 2.5 x
109 / L، الحبيبات 1.0 x
109 / L، مستوى الهيموغلوبين من 100 جم / لتر.
في الآونة الأخيرة، مفهوم البيولوجية السيولوجية والجزيئية
مغفرة. - المسرح
الحد الأدنى من المرض المتبقي (المتبقي). - recurd
الأمراض (نخاع العظام، زيادة الحركة. - طرفية
المسرح.
علاج او معاملة
قبل بدء العلاج، سريرية كاملة
فحص المريض لتقييم حالة علم الأمراض المصاحبة
القلب والأوعية الدموية، الجهاز التنفسي، النظم البولية، الجهاز العصبي المركزي.
ويشمل اختبار دم كيمياء حيواني كامل، coagologram، الفحص
التهاب الكبد B و C، فيروس نقص المناعة البشرية، فيروسات مجموعة الهربس. الموجات فوق الصوتية للأجهزة
تجويف البطن، دراسة الأشعة السينية الصدر / الكمبيوتر
التصوير المقطعي الصدر، ECG / ECHO القلب، CT / MRI Head، التفتيش
طبيب الأعصاب، المفروك و.د. كل هذا ضروري للاختيار الصحيح للعلاج و
منع المضاعفات.
طرق العلاج
المرضى الذين يعتمدون IML يعتمدون على نوع المرض، والعوامل النذيرية، والعمر
المريض، وكذلك علم الأمراض ذات الصلة ويمكن تقسيمها إلى
من المحتمل أن شفاء الأساليب العلاجية والدعم العلاج.
دعم I
العلاج الأعراض
مؤسسة
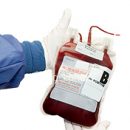
علاج OML هو العلاج الداعم، والذي يتضمن علاج الإصابات Intercurrent، uRsural
الحفريات، العلاج البدائل مع مكونات الدم، وكذلك العلاج
علم الأمراض المصاحبة.
مرتكز على
دعم العلاج من المرضى الذين يعانون من MDS الأكاذيب استبدال العلاج
مكونات الدم. المرضى الذين يعانون من انخفاض خطر التنمية OML فقر الدم يمكن أن يكون
السريرية الرئيسية مشكلة ذات معنى. نظرية الاستبدال
يسهل أعراض فقر الدم، وبالتالي، هو علاج مهم.
تكرار
عمليات النقل تعتمد على حالة المريض، وشدة فقر الدم، وكذلك
علم الأمراض المصاحبة، وخاصة الحاجة إلى مكونات تفيض
الدم عند التطور في نزيف المريض. نتيجة العلاج بديل
هي زيادة في مستوى الهيموغلوبين، والدراسات التي تظهر,
لديه ارتباط إيجابي مع مؤشر جودة الجودة.
نقل
يتم تنفيذ كتلة الصفائح الدموية في الحالات التي يكون فيها عدد الصفائح الدموية
منخفضة للغاية و / أو هناك نزيف خطير. تحت التطوير
التخثر (الانتهاكات في نظام تخثر الدم، على سبيل المثال، تخفيض المستوى
الفيبرينوجين أو العوامل المعقدة البروثرومبين) إجراء استبدال
العلاج من مكونات البلازما الدم أو
مؤرجة prepartes (novosvlen، prombomoplex والعلاقات العامة.في
من المحتمل أن شفاء الأساليب العلاجية
-
 للسيطرة على أعراض المرض أو علاج IML في المرضى الشباب
للسيطرة على أعراض المرض أو علاج IML في المرضى الشباب
العلاج الكيميائي المكثف لتدمير استنساخ المرضية
الخلايا والوصول إلى مغفرة طويلة. هذه طريقة العلاج لديها
آثار جانبية كبيرة، مثل تساقط الشعر، ومظهر التهاب الفم
تجويف عن طريق الفم، الغثيان، القيء، ظهور البراز السائل. بالإضافة إلى هذه الجانب
الظواهر، العلاج الكيميائي له آثار ضارة وصحية
الخلايا التي تتطلب إقامة طويلة في الدم
الإدارات. في هذا الوقت، يتم المريض على خلية الدم
يتم وصف كتلة الخثرة، الأدوية المضادة للجراثيم لمكافحة
عدوى. إذا كان العلاج الكيميائي التعريفي يوفر سيطرة كافية
الخلايا المرضية (حالة مغفرة)، ثم استعادة طبيعية
يجب أن تبدأ خلايا الدم في غضون بضعة أسابيع. ومع ذلك، حتى في الحالات
يمكن إرجاع مرض العلاج الناجح — تكرر. - الوحيد
طريقة المعروفة للعلاج قادرة على شفاء معظم المرضى الذين يعانون من OML,
هو زرع الجذعية المكونة من allogeneic (المانح)
خلايا. يجب أن يؤخذ في الاعتبار أن هذا إجراء معقد من المخاطر المرتبطة بالمخاطر
مضاعفات مبكرة ومتأخرة. تعتمد نتائج العلاج على درجة التوافق (توافق HLA) من المانح والمريض
(المستلم)، وكذلك في توافر خلايا الجهات المانحة المناسبة (توافر
إخوان الدم المتوافق مع / أو الأخوات، توفر بنك المانحين). هكذا
الطريقة التي توجد بها شهادة صارمة وموانع لهذا النوع من العلاج:
إنها مناسبة لتلك الحالات عندما يكون المرضى قادرين على النقل
زراعة الخلايا الجذعية والحصول على جهة مانحة مناسبة والإجابة على العلاج الكيميائي. - يذاكر
أظهرت آليات تطوير MDS / IML الثانوية، التي أجريت في السنوات الأخيرة,
أنه لهذا الأمراض بهذا الأمراض يتميز بفرق منطقة المروج
بعض الجينات - oncosuppressors، مما يؤدي إلى «الصمت» هذه الجينات I
انتشار الخلايا والتحولات الورم في IML. على أساس هذه المعرفة
تم تطوير وكلاء ما يسمى بالضغط الذين يساهمون
الحمض النووي spomettylation، مما تسبب في التعبير في وقت سابق «معاق» جينوف.
في مايو 2004، الإدارة
الولايات المتحدة الأمريكية للسيطرة على الغذاء والدواء (إدارة الغذاء والعقاقير، FDA) تصدر إذنا للاستخدام
إعداد حقن الأزليطيدين (فيفاظة) لعلاج جميع أنواع MDS. في الاتحاد الروسي
تمت الموافقة على الدواء للاستخدام في عام 2010، بما في ذلك لعلاج كل من MDS و IML. أظهرت نتائج الدراسة ذلك
يطيل Azacytidin الحياة إلى المرضى الذين يعانون من سرطان الدم النذوي الحاد,
زرع الخلايا الجذعية المقررة / المكثف
العلاج الكيميائي. تشير الدراسات إلى أن معدل البقاء على قيد الحياة من المرضى الذين يعانون من OML دون علاج حديث هو 1.6
أشهر، في حين يزيد أزاسيتيدين من عمر مع IML
11.1 شهرا، امتلاك مواتية
صورة الأمان. بجانب,
الدواء، مع مؤهلات كافية من العاملين الطبيين، مايو
تطبيق محمور.
وفقا للبروتوكولات المعتمدة في روسيا، فإن علاج المرضى IML، والتي ليست كذلك
مناسبة للكثف
يتم إجراء العلاج الكيميائي وعمل OML الثانوي بجرعات منخفضة من السيتارابين و / أو مع
باستخدام العلاج الداعم [واحدحدوث. مثل هذا العلاج
يحسن نوعية حياة المرضى، ولكن لا يزيد من حياتهم
بالمقارنة مع المسار الطبيعي للمرض. أثناء الاستخدام
Azacitidine في هذه الفئة من المرضى يمكن أن يغير التدفق بشكل جذري
الأمراض (الجدول 1).
الطاولة
واحد. متوسط البقاء على قيد الحياة في مريض IML، اعتمادا على العلاج (غير مباشر
البيانات المقارنة).
| بدون علاج | دعم العلاج | جرعات منخفضة من السكتارابين | azacytidin | |
| OML، بما في ذلك عدد OML S عدد الانفجارات في المايلوجرام 20-30٪ | 1،6 | 13،4 | 17.0 | 24.5 |
متوسط البقاء على قيد الحياة للمرضى مع OML (20-30٪ من الانفجارات),
تلقي Azacytidine، يزيد إلى 24.5 شهرا. في الوقت نفسه، الاختلافات في المجموعة
Azacytidine مع مجموعات من العلاج الداعم وجرعات منخفضة من السيتارابين
موثوقة إحصائيا (ص = 0.045)، بغض النظر عن العمر أو كيروت، و
أشهر اختيارية من الحياة 11.1 و 7.5 على التوالي (متوسط
البقاء على قيد الحياة في مجموعة العلاج الداعمة يساوي 13.4 وفي المجموعة المنخفضة
جرعات السيتارابين — 17.0 شهرا) (تحليل أبحاث البيانات III المرحلة AZA-001) [2حدوث. بعد عامين، كان 50.8٪ من المرضى في المجموعة على قيد الحياة
Azacitidine، الذي هو أكثر من 2 مرات أكثر من مجموعات المقارنة (26.2٪). إلى عن على
مقارنة — المرضى الذين يعانون من OML الذين لا يتلقون العلاج الحديث (طبيعي
يموت مسار المرض) في غضون 7 أسابيع من التشخيص.
 للمرضى الذين يعانون من IML، وليس
للمرضى الذين يعانون من IML، وليس
العلاج الكيميائي المكثف / زرع الخلايا الجذعية، العلاج
قد يكون Azacytidine الوسيلة الوحيدة لطفل الحياة و
المساعدة في تحقيق مغفرة طويلة. في دراسة AZA-001 في مجموعة Azacitidine على استجابة العلاج
(المعايير IWG
2000) بلغ 29٪ من المرضى (إجابة كاملة وجزعة)، 49٪ — حقق
تحسين الدم. الاختلافات مع مجموعات المقارنة («دعم
علاج نفسي», «جرعات منخفضة من السكتارابين»موثوقة إحصائيا (5 و 12٪ و 31 و 25٪
على التوالى). كان الوقت لتطور المرض 14.1 أشهر
مجموعة «azacytiddine» و 8.8 أشهر في مجموعات المقارنة (P = 0.047). مدة
كانت استجابة الدم 13.6 شهرا على الأزليطين بالمقارنة مع
5.2 أشهر على العلاج المستخدم تقليديا (P = 0.002).
في المرضى الذين يعانون من MDS و IML الذي تلقى
وقد لوحظ العلاج الاسكيتيدين احتمال أعلى للاستقلال من
عمليات نقل كتلة كريات كريات الحمراء: 45٪ من المرضى أصبحوا مستقلين عن
hemotransphus، بينما على الأوضاع التقليدية — 11٪ فقط (ص < 0.0001).
وهكذا، علاج أسكيتيدين للمرضى OML (20-30٪ من الانفجارات)
رافق ليس فقط من خلال متوسط العمر المتوقع والإجمالي
الترددات الشفاء مقارنة بدعم العلاج والجرعات المنخفضة من السكتارابينا,
ولكن أيضا ارتفاع تحسين الدم والاستقلال
عمليات نقل. المرضى الذين يعانون من MDS عالية المخاطر العلاج Azacytidine
يرافقه زيادة في الوقت المناسب قبل التحول إلى OML (17.8 شهرا مقابل 11.5 شهرا، ص<0.001).
يتم تضمين Azacytidin في البروتوكولات الدولية للعلاج
المرضى الذين يعانون من متلازمة myelodsplastic و IML في المرضى الذين تزيد أعمارهم عن 60 عاما.
الولايات المتحدة الأمريكية: في الدليل الوطني لعمل العلاج
شبكة الأورام (الوطني سرطان شامل شبكة, NCCN, الولايات المتحدة الأمريكيةفي (2010) ينصح Azacytidine للتطبيق
المرضى الذين تزيد أعمارهم عن 60 عاما الذين ليسوا مرشحين لمرئي للغاية
العلاج الكيميائي. وترد التوصيات بمستوى عال من الأدلة.
ل
الظواهر غير المرغوب فيها من 3-4 درجات النامية ضد خلفية علاج الأزليطين,
علاج دموية (71.4٪)، بما في ذلك القطب الحريق (85٪)، العدلات
(91٪) وفقر الدم (5